Atenção
Fechar
O diagrama da Fig. 207 é de natureza metaestável ou de pseudo-equilíbrio, pois, com o tempo, pode ocorrer decomposição do Fe3C em ferro e carbono, este último na forma de grafita.
Essa decomposição é acelerada pela presença de silício, de modo que convém estudar o efeito desse elemento no diagrama de equilíbrio Fe-C. Trata-se, assim, de estudar um diagrama ternário, o que pode ser feito tomando-se secções do diagrama Fe-C-Si, para teores determinados de silício. A Fig. 211 (295) mostra secções para teores de silício de 2,3%, 3,5%, 5,2% e 7,9%. Os dois primeiros correspondem a ligas Fe-C-Si de maior uso prático. Nas figuras são mostradas apenas as linhas de transformação para temperatura, elevadas, a partir de 1000°C.
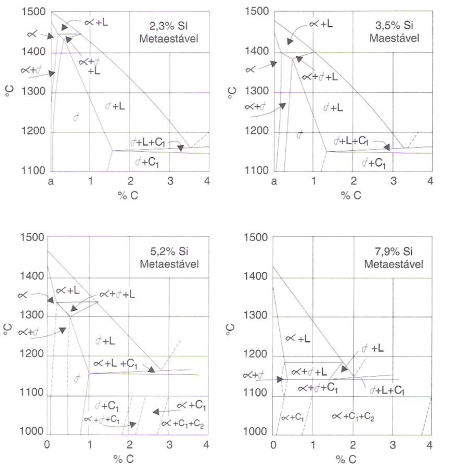
Fig. 211 – Diagramas de equilíbrio metaestáveis Fe-C-Si para quatro diferentes teores de silício
Pela sua observação verifica-se que a principal alteração refere-se à composição do eutético, o qual diminui à medida que aumenta o teor de silício. Ao mesmo tempo, nota-se que a reação do eutético ocorre num intervalo de temperatura, ao contrário do que acontece no diagrama binário Fe-C, onde tal reação se dá a uma temperatura praticamente constante.
Sob o ponto de vista prático, a utilização e interpretação dos fenômenos de transformação dos diagramas ternários são relativamente complexas.
A figura 212 mostra as faixas dos teores de carbono e de silício das ligas ferrosas. A linha tracejada inferior define o limite superior de teor de carbono como o limite da solubilidade do carbono na austenita.
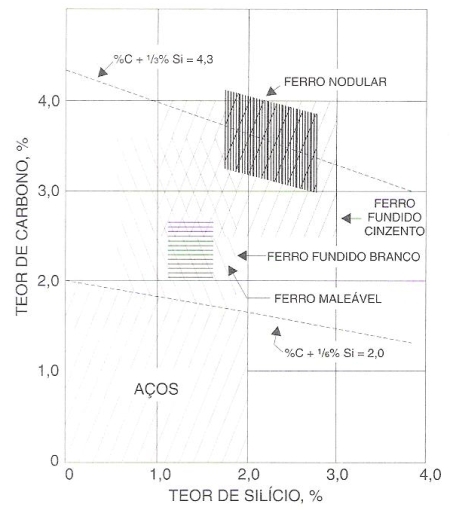
Fig. 212 – Faixa aproximada de quantidades de carbono e silício nas ligas ferrosas
No caso dos ferros fundidos tomados como ligas ternárias, utiliza-se um conceito ou fórmula que possibilita levar em consideração o efeito do silício nas transformações estruturais e, portanto, nas propriedades dos ferros fundidos, em que o silício está presente em teores relativamente elevados.
Esse conceito é o do “carbono equivalente” e é representado pela fórmula
C. E. = % C + 1/3 (% Si + % P)
Deixando de lado o fósforo, cuja influência nessas ligas será estudada mais adiante, ter-se-ia apenas:
C. E. = % C + 1/3 (% Si)
A fórmula indica que o efeito do silício corresponde ao de um terço do efeito do carbono. Por exemplo, tomando-se na Fig.211 uma liga com 2,3% de Si, verifica-se que o ponto eutético corresponde a cerca de 3,6%. Aplicando-se a fórmula ter-se-ia:
C. E. = 3,6 + 2,3/3 = 4,3% aproximadamente
Do mesmo modo, na liga com 3,5% de silício, onde o eutético foi deslocado para cerca de 3,20% de carbono, ter-se-ia:
C. E. = 3,2 + 3,5/3 = 4,3 aproximadamente
Em resumo, as ligas com 3,6% de carbono e 2,3% de silício e com 3,2% de carbono e 3,5% de silício comportam-se como ligas eutéticas e apresentam, teoricamente, à temperatura ambiente, uma estrutura ledeburítica.
Na verdade, além do efeito que o silício exerce ao deslocar o eutético para teores mais baixos de carbono (essa influência também se faz sentir nos aços, cujo teor de carbono do eutetóide diminui à medida que aumenta o teor de silício), uma outra característica desse elemento, fundamental sob o ponto de vista de estrutura e propriedades mecânicas, relaciona-se com sua tendência grafitizante, ou seja, promover a decomposição do Fe3C em ferro e carbono, este último sob a forma de grafita lamelar.
Tomando-se a secção correspondente a 2,0% de Si de um diagrama completo Fe-C-Si, como mostra a Fig. 213, verifica-se a existência de três fases (áreas achuradas), uma das quais é grafita.
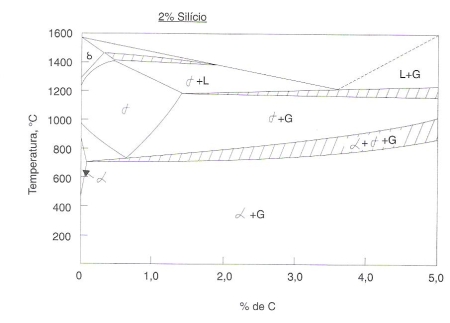
Fig. 213 – Secção vertical do sistema Fe-C-Si a um teor constante de 2% de Si, mostrando, em achurado, as áreas de três fases.
Como ou quando se forma a grafita?
Lembre-se de que o diagrama de equilíbrio Fe-C é de natureza metaestável: a rigor, trata-se de um diagrama Fe-Fe3C. O equilíbrio estável corresponde, de fato, à liga ferro-grafita, ou seja, as condições de equilíbrio são tais que ocorre a decomposição do Fe3C em Fe e C, este último na forma de grafita.
Essa decomposição depende da velocidade de resfriamento e da presença de determinados elementos de liga.
Ao solidificar um ferro fundido cinzento hipoeutético, por exemplo, com 3% de carbono 2,3% de silício, resultam, em primeiro lugar, cristais primários de austenita, cuja quantidade aumenta com o decréscimo da temperatura. A cerca de 1150°, o líquido remanescente solidifica com um teor de carbono de aproximdamente 3,6% (Fig. 211). Nesse momento, por reações complexas, ainda não devidamente explicadas, ocorre em grande parte a grafitização. Admite-se, entretanto, que, no curto intervalo de tempo em que ocorre a solidificação final, fica estabelecida a quantidade, a forma e a distribuição da grafita.
Abaixo da temperatura de solidificação, no exemplo considerado, têm-se, pois, dendritas de austenita, cujo teor de carbono decresce com a queda da temperatura, formando uma matriz em que estão distribuídas lamelas de grafita. O carbono, que é precipitado da austenita, aparece como perlita e em parte como grafita livre. A quantidade desta depende, como já mencionou, da velocidade de resfriamento e do teor de silício.
Ao ultrapassar a última linha de transformação, corresponde à temperatura do eutetóide, a austenita remanescente passa a perlita e a estrutura da liga é constituída de perlita com lamelas de grafita, podendo, ainda, com resfriamento mais lento, a perlita decompor-se parcialmente em ferrita e grafita. A estrutura consistirá, então, de perlita, ferrita e lamelas de grafita (Fig. 214). Essa é uma das estruturas comuns em ferros fundidos cinzentos de maior utilização comercial.
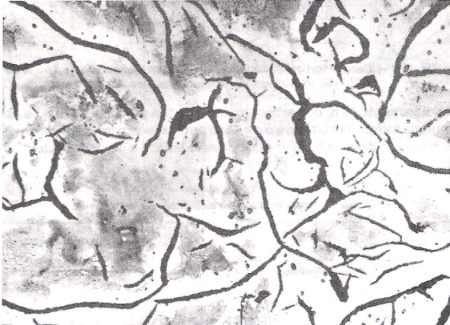
Fig. 214 – Estrutura de ferro fundido cinzento do tipo hipoeutético, mostrando os constituintes perlita, ferrita e veios de grafita. Ataque: picral. Aumento: 100x. (Gentileza do Instituto de Pesquisas Tecnológicas de São Paulo).